ラクオリア創薬産学協同研究センター
(薬効解析部門、新薬創成科学部門)

教員紹介
センター長

教授
澤田 誠
SAWADA Makoto
薬効解析部門

特任准教授
須軽 英仁
SUGARU Eiji

特任准教授
上部 健一郎
UWABE Kenichiro

特任助教
平尾 顕三
HIRAO Kenzo

特任助教
Andrea R. J. Anas
Andrea R. J. Anas
新薬創成科学部門

特任准教授
森田 幹雄
MORITA Mikio

特任助教
川村 清
KAWAMURA Kiyoshi

特任助教
山岸 竜也
YAMAGISHI Tatsuya
研究内容
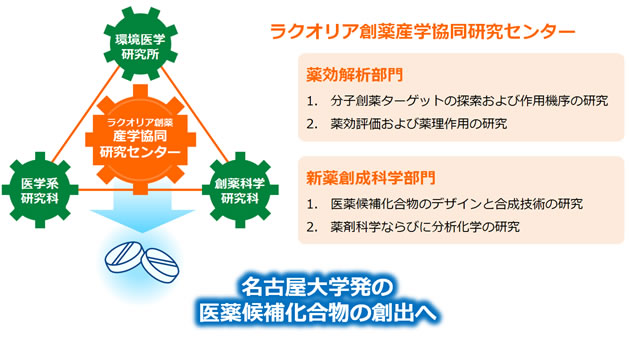
ラクオリア創薬産学協同研究センターは、薬効解析部門と新薬創成科学部門の2つの部門からなり、ラクオリア創薬株式会社と名古屋大学が共同で新薬を創成するため新たに名古屋大学の中に設置されました。環境医学研究所を受入部局とし、医学系研究科及び創薬科学研究科とは研究チームを設立、各部局との強固なトライアングル連携体制を構築することにより、部局横断的な創薬研究を可能としています。
薬効解析部門
創薬ターゲット分子に応じて、薬効を評価する薬理モデルを確立し、医薬候補化合物の評価検証を実施しています。具体的には、イオンチャネルを始めとする創薬分子標的を特定し、ロボットを用いた化合物ライブラリーのハイスループットスクリーニングを立ち上げ、新薬創成科学部門において新規合成された化合物のin vitro/in vivo薬理・ADMET(Absorption, Distribution, Metabolism, Excretion, and Toxicity)評価を行っています。
新薬創成科学部門
化合物ライブラリーから見いだされたヒット化合物を基に、医薬候補化合物のデザインと合成を実施しています。新規化合物のデザインにおいては、標的分子の構造情報や既知リガンドの情報を基に、計算化学的アプローチも取り入れています。合成した化合物は、薬効解析部門において薬理評価され、そのin vitro/in vivo試験データを系統的に解析し、構造活性相関研究(SAR: Structure-Activity Relationship)を展開しています。また、医薬候補化合物の物性・薬剤科学的評価も行っています。
研究業績
- Nishinaka A, Tanaka M, Ohara K, Sugaru E, Shishido Y, Sugiura A, Moriguchi Y, Toui A, Nakamura S, Shimada K, Watanabe S, Hara H, Shimazawa M. TRPV4 channels promote vascular permeability in retinal vascular disease. Experimental Eye Research 228: 109405,2023.
- Mori Y, Tsuchihira A, Yoshida T, Yoshida S, Fujiuchi A, Omi M, Isogai Y, Sakaguchi T, Eguchi S, Tsuda T, Kato K, Ohashi K, Ouchi N, Park HM, Murohara T, Takefuji M. Corticotropin releasing hormone receptor 2 antagonist, RQ-00490721, for the prevention of pressure overload-induced cardiac dysfunction. Biomed. Pharmacother. 146: 112566, 2022.
- Tanaka S, Morita M, Yamagishi T, Madapally HV, Hayashida K, Khandelia H, Gerle C, Shigematsu H, Oshima A, Abe K. Structural basis for binding of potassium-competitive acid blockers to the gastric proton pump. J. Med. Chem. 65: 7843-53, 2022.
- Oya M, Suzuki H, Anas ARJ, Oishi K, Ono K, Yamaguchi S, Eguchi M, Sawada M. LC-MS/MS imaging with thermal film-based laser microdissection. Anal Bioanal Chem. 410: 491-499, 2018.
- Okumura Y, Yamagishi T, Nukui S, Nakao K. Discovery of AAT-008, a novel, potent, and selective prostaglandin EP4 receptor antagonist. Bioorg. Med. Chem. Lett. 27: 1186-1192, 2017.
- Morita H, Mochiki E, Takahashi N, Kawamura K, Watanabe A, Sutou, T, Ogawa, A, Yanai, M, Ogata, K, Fujii, T. Effects of 5-HT2B, 5-HT3 and 5-HT4 receptor antagonist on gastrointestinal motor activity in dogs. World J. Gastroenterol. 19: 6604-6612, 2013.
- Kosteli A, Sugaru E, Hammerle G, Martin J, Lei J, Zechner R, Ferrante AW Jr. Weight loss and lipolysis promote a dynamic immune response in murine adipose tissue. J. Clin. Invest. 120: 3466-79, 2010.
- Obstfeld AE*, Sugaru E*, Thearle M, Francisco AM, Gayet C, Ginsberg HN, Ables EV, Ferrante AW Jr. C-C chemokine receptor 2 (CCR2) regulates the hepatic recruitment of myeloid cells that promote obesity-induced hepatic steatosis. Diabetes 59: 916-25, 2010.
- Onoue S, Kawamura K, Igarashi N, Zhou Y, Fujikawa M, Yamada H, Tsuda Y, Seto Y, Yamada S. Reactive oxygen species assay-based risk assessment of drug-induced phototoxicity: classification criteria and application to drug candidates. J. Pharm. Biomed. Anal. 47: 967-972, 2008.
