組織移行性細胞技術、イメージング手法の開発
- (1)組織移行性細胞の解明とその性質を利用した薬物の標的化や疾患治療への応用
- (2)画期的な生体イメージング法の開発
-小動物用MRIによる遺伝子発現の生体内観察
-広帯域近赤外光源による生体イメージング
-ミクログリアの毒性転換の生体イメージング - (3)光による細胞活性化制御
(1)組織移行性細胞の解明とその性質を利用した薬物の標的化や疾患治療への応用
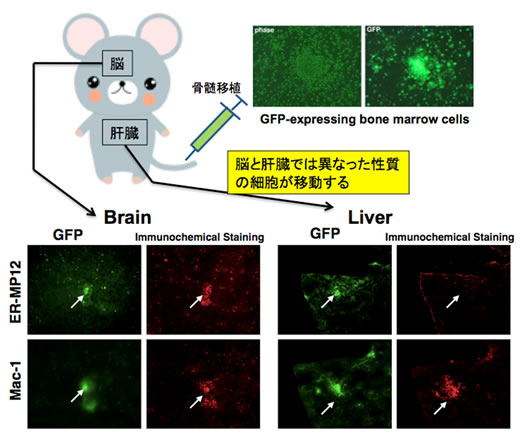
私たちは骨髄細胞の中に微量ではあるものの、ミクログリアと同様に脳選択的に移行する細胞が存在することを明らかにしました。これらの細胞は、正常マウス脳内において未分化な性質を維持していますが、脳内で生じる傷害や炎症に応答して分化・集積する性質を有しています。これらの細胞が脳の疾患に対してどのような応答や役割を示すのか検討を行っています。また、脳だけではなく特定末梢組織に対しても選択的移行性を示す細胞が存在することも明らかにしており、これらの細胞の活性化を制御することでさまざまな疾患における細胞間相互作用について検討し、将来的な治療応用を目指しています。
(2)画期的な生体イメージング法の開発
私たちは小動物用MRIや光イメージング技術、PET、顕微イメージングなどの技法を用いて、動物の個体・細胞レベルで生じる変化を低侵襲的に可視化する技術の開発やその技術を応用し生体現象を解明する研究を行っています。
小動物用MRIによる遺伝子発現の生体内観察:鉄貯蔵タンパク質フェリチンがMRIのT2強調画像において陰性造影効果を示すことに着目し、フェリチンをレポーターとして特定プロモーター制御下で細胞に発現させることで、生体における細胞の動態を遺伝子発現に基づいて可視化する手法を開発しました。

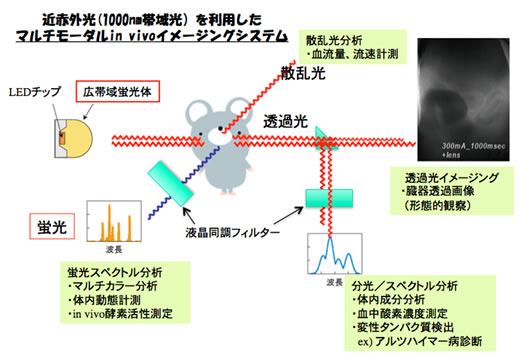
広帯域近赤外光源による生体イメージング:工学研究科との共同研究で新規な広帯域蛍光体を用いて生体透過性の近赤外光をつかって生体機能の画像化法を開発しています。光のいろいろな性質を利用する事によって生体成分の分析や病態の観察,疾患による生化学的変化の分析などが可能となります。
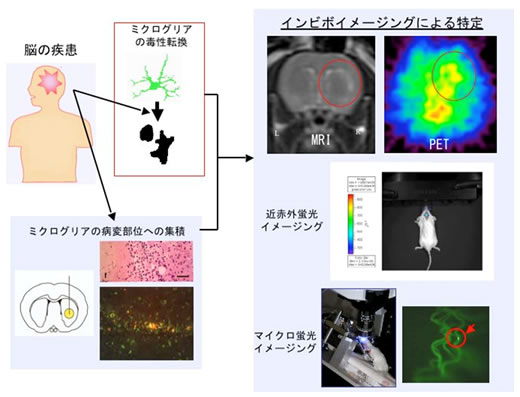
ミクログリアの毒性転換の生体イメージング:ミクログリアは種々の疾患により神経細胞などが変性すると活性化され、疾患部分に集積しその一部が増殖します。活性化して集積するミクログリアには損傷して回復不可能な機能不全を起こした細胞を攻撃して排除する細胞(細胞傷害性ミクログリア)と、傷害から細胞を保護する役割の細胞(保護的ミクログリア)があり、このミクログリアの状態をin vivoで識別できる手段があればミクログリアが活性化していることが知られているアルツハイマー病やパーキンソン病、脳梗塞、脳腫瘍などの種々の脳疾患の早期診断が可能となると考えられます。活性化したミクログリアにはいくつかの特徴的な変化があり,そのうちのひとつとして末梢性ベンゾジアゼピン受容体(PBR)へのリガンドの結合性の変化が病変部に連関したミクログリアの活性化状態と密接に関連している可能性が示唆されています。私たちは藤田保健衛生大学医学部放射線科、国立長寿医療研究センター、カナダトロント大学、イタリアバーリ大学との共同研究で傷害性と保護的なミクログリアが識別できるイメージングリガンド(PETリガンドや蛍光プローブ)について研究を行っています。この研究により傷害性と保護的なミクログリアが区別できる様になると病態形成の早期検出だけでなく重症度や予後の予測までできると考えられます。
(3)光による細胞活性化制御
光感受性イオンチャネルを脳細胞に発現させ、光照射によって細胞の状態を制御して脳や生体の機能を調節する研究を行っています。
クラミドモナス藻由来のChannelrhodopsin-2(ChR2)と呼ばれる膜タンパク質は、青色光に対して選択的に応答するイオンチャネルとして知られています。ChR2は、哺乳類の細胞に存在するRhodopsin群とは異なり基質を介さないため、光刺激によって直接イオンチャネルの開閉を制御することができます。近年、ChR2を発現させた神経細胞を用いた神経回路網に関する研究が盛んに行われていますが、私たちは神経細胞だけでなく遺伝子導入したグリア細胞を作製し、特定の細胞を活性化させることで脳機能を人為的に調節する技術を開発しています。